Η Bristol Myers Squibb ανακοίνωσε ότι η Ευρωπαϊκή Επιτροπή ενέκρινε το nivolumab ως μονοθεραπεία για την επικουρική θεραπεία ενηλίκων και εφήβων ηλικίας 12 ετών και άνω με μελάνωμα σταδίου IIB ή IIC οι οποίοι έχουν υποβληθεί σε πλήρη χειρουργική εξαίρεση του όγκου, με βάση τα αποτελέσματα της μελέτης CheckMate -76K.
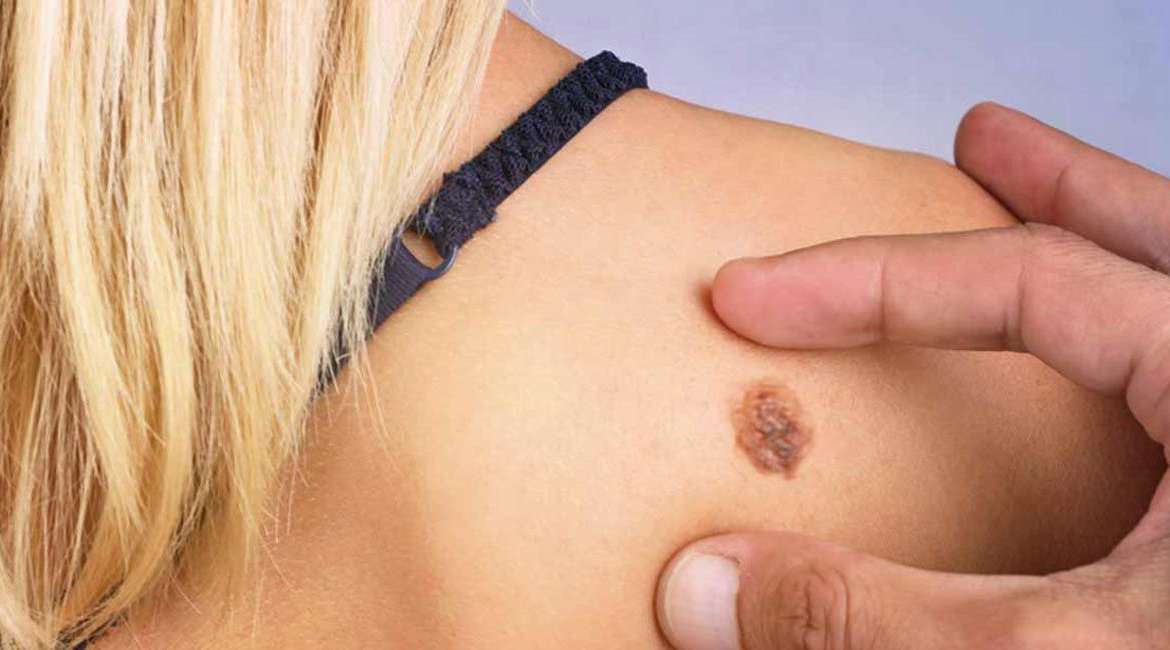
Το μελάνωμα είναι μία μορφή καρκίνου του δέρματος που χαρακτηρίζεται από ανεξέλεγκτη ανάπτυξη των κυττάρων που παράγουν μελανίνη (μελανοκύτταρα). Το μεταστατικό μελάνωμα αποτελεί την πιο θανατηφόρο μορφή της νόσου και παρουσιάζεται όταν ο καρκίνος εξαπλωθεί σε άλλα όργανα πέραν της επιφάνειας του δέρματος. Επιπλέον, ο Παγκόσμιος Οργανισμός Υγείας εκτιμά ότι έως το 2035 τα περιστατικά μελανώματος σε παγκόσμιο επίπεδο θα ανέλθουν σε 424.102 και οι θάνατοι σε 94.308. Το μελάνωμα είναι μια ιάσιμη νόσος εφόσον διαγνωστεί και αντιμετωπιστεί στα αρχικά στάδια, ωστόσο οι πιθανότητες επιβίωσης των ασθενών μειώνονται όσο εξελίσσεται η νόσος.
Η συγκεκριμένη έγκριση επεκτείνει την έγκριση που παραχώρησε η Ευρωπαϊκή Επιτροπή το 2018 βάσει των αποτελεσμάτων της μελέτης CheckMate -238. Το nivolumab είναι πλέον εγκεκριμένο για χρήση στην Ευρωπαϊκή Ένωση ως μονοθεραπεία για την επικουρική θεραπεία ενηλίκων και εφήβων ηλικίας 12 ετών και άνω με μελάνωμα σταδίου IIB ή IIC, με συμμετοχή των λεμφαδένων ή μεταστατική νόσο, οι οποίοι έχουν υποβληθεί σε πλήρη εξαίρεση του όγκου. Το nivolumab είναι ο μοναδικός αναστολέας του PD-1 ο οποίος, χάρη στις δύο εγκρίσεις, ενδείκνυται ως επικουρική θεραπεία για μελάνωμα σταδίου IIB, IIC, III καθώς και σταδίου IV το οποίο έχει εξαιρεθεί χειρουργικά.
«Οι ασθενείς με μελάνωμα σταδίου IIB ή IIC διατρέχουν υψηλό κίνδυνο υποτροπής μετά τη χειρουργική επέμβαση, με δυνητικά σημαντικές επιπτώσεις για τους ασθενείς», δήλωσε ο Peter Mohr, MD, Αρχίατρος και Επικεφαλής στο Κέντρο για τον Καρκίνο του Δέρματος του Τμήματος Δερματολογίας στο νοσοκομείο Elbe-Kliniken στο Μπουξτεχούντε της Γερμανίας. «Η συγκεκριμένη έγκριση ενισχύει το όφελος που μπορεί να προσφέρει το nivolumab όταν χρησιμοποιείται μετά τη χειρουργική εξαίρεση, προλαμβάνοντας ενδεχομένως την υποτροπή της νόσου».
Η απόφαση της Ευρωπαϊκής Επιτροπής βασίζεται σε αποτελέσματα από τη μελέτη Φάσης 3 CheckMate -76K, στο πλαίσιο της οποίας, με ελάχιστη παρακολούθηση 7,8 μηνών, το nivolumab μείωσε τον κίνδυνο υποτροπής ή θανάτου σε ασθενείς με μελάνωμα σταδίου IIB ή IIC κατά 58% έναντι εικονικού φαρμάκου (αναλογία κινδύνου [HR] 0,42· 95% CI: 0,30-0,59· p<0,0001). Το προφίλ ασφάλειας του nivolumab ήταν αντίστοιχο με το προφίλ που αναφέρθηκε σε προηγούμενες μελέτες.
Η μελέτη CheckMate -76K συμπεριλαμβάνεται στο πρόγραμμα ανάπτυξης της Bristol Myers Squibb το οποίο διερευνά τη χρήση του nivolumab και συνδυαστικών θεραπειών με βάση το nivolumab σε αρχικά στάδια του καρκίνου.
«Χάρη σε αυτή την έγκριση, είμαστε πλέον σε θέση να προσφέρουμε στους ασθενείς στην Ευρωπαϊκή Ένωση, οι οποίοι πάσχουν από μελάνωμα σταδίου IIB ή IIC το οποίο έχει εξαιρεθεί χειρουργικά, μία αποτελεσματική θεραπευτική επιλογή που μείωσε σημαντικά τον κίνδυνο υποτροπής της νόσου», δήλωσε η Gina Fusaro, Ph.D., αντιπρόεδρος, επικεφαλής του παγκόσμιου προγράμματος στην Bristol Myers Squibb. «Η έγκριση ενισχύει τη μακροχρόνια δέσμευσή μας να προσφέρουμε καινοτόμα φάρμακα στους ασθενείς σε κάθε στάδιο του καρκίνου, συμπεριλαμβανομένης της πρώιμης νόσου. Θέλουμε να ευχαριστήσουμε τους ασθενείς, τους ερευνητές και τους θεράποντες ιατρούς που συμμετείχαν σε όλες τις φάσεις της διαδικασίας συμβάλλοντας ώστε να γίνει πραγματικότητα αυτή η πρόσθετη επιλογή για τους ασθενείς».
Η έγκριση της Ευρωπαϊκής Επιτροπής ισχύει για όλα τα κράτη μέλη της Ευρωπαϊκής Ένωσης, καθώς και για την Ισλανδία, το Λιχτενστάιν και τη Νορβηγία. H κεντρική Άδεια Κυκλοφορίας δεν περιλαμβάνει έγκριση στη Μεγάλη Βρετανία (Αγγλία, Σκωτία και Ουαλία).