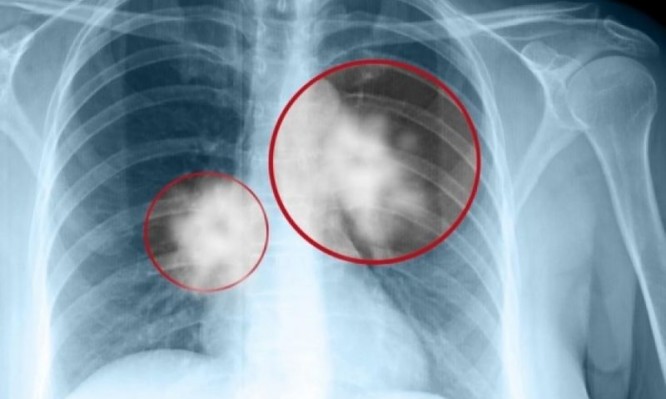
Η Bristol Myers Squibb (NYSE: BMY) ανακοίνωσε ότι η Επιτροπή Φαρμακευτικών Προϊόντων για Ανθρώπινη Χρήση (CHMP) του Ευρωπαϊκού Οργανισμού Φαρμάκων (EMA) συστήνει την έγκριση της θεραπείας nivolumab με ipilimumab σε συνδυασμό με δύο κύκλους πλατινούχου χημειοθεραπευτικού σχήματος για την πρώτης γραμμής θεραπεία του μεταστατικού μη μικροκυτταρικού καρκίνου του πνεύμονα (NSCLC) σε ενήλικες των οποίων οι όγκοι δεν φέρουν μετάλλαξη ευαισθητοποίησης EGFR ή μετατόπιση ALK. Η Ευρωπαϊκή Επιτροπή, η οποία είναι αρμόδια για την έγκριση φαρμάκων για την Ευρωπαϊκή Ένωση, θα αξιολογήσει τη σύσταση της Επιτροπής Φαρμακευτικών Προϊόντων για Ανθρώπινη Χρήση (CHMP).
«Η θετική γνωμοδότηση της Επιτροπής Φαρμακευτικών Προϊόντων για Ανθρώπινη Χρήση (CHMP) αντικατοπτρίζει τη δυνατότητα που διαθέτει η θεραπεία nivolumab με ipilimumab σε συνδυασμό με δύο κύκλους χημειοθεραπείας να παρατείνει τη ζωή των ασθενών σε όλες τις υποομάδες του μεταστατικού μη μικροκυτταρικού καρκίνου του πνεύμονα, ο οποίος αποτελεί έναν εξουθενωτικό τύπο καρκίνου, όπου συνεχίζει να υφίσταται ανεκπλήρωτη ιατρική ανάγκη», δήλωσε ο Abderrahim Oukessou, M.D., αντιπρόεδρος ανάπτυξης του τμήματος καρκίνου του θώρακα της Bristol Myers Squibb. «Προσβλέπουμε με ανυπομονησία στην απόφαση της Ευρωπαϊκής Επιτροπής και ευελπιστούμε ότι σύντομα θα προσφέρουμε αυτή την καινοτόμο προσέγγιση διπλής ανοσοθεραπείας στους ασθενείς στην ΕΕ, οι οποίοι μπορεί να ωφεληθούν».
Η Επιτροπή Φαρμακευτικών Προϊόντων για Ανθρώπινη Χρήση (CHMP) υιοθέτησε θετική γνωμοδότηση με βάση τα αποτελέσματα από τη μελέτη Φάσης 3 CheckMate -9LA, η οποία πέτυχε το πρωτεύον καταληκτικό σημείο της υπεροχής της συνολικής επιβίωσης (OS). Το προφίλ ασφάλειας της θεραπείας nivolumab με ipilimumab σε συνδυασμό με δύο κύκλους χημειοθεραπείας ήταν αντίστοιχο με το γνωστό προφίλ ασφάλειας της ανοσοθεραπείας και της χημειοθεραπείας στη θεραπεία πρώτης γραμμής του μη μικροκυτταρικού καρκίνου του πνεύμονα (NSCLC). Τα πλήρη δεδομένα από τη μελέτη CheckMate -9LA ανακοινώθηκαν σε μια συνεδρία προφορικών παρουσιάσεων στο πλαίσιο του Διαδικτυακού Επιστημονικού Προγράμματος του Συνεδρίου της Αμερικανικής Εταιρείας Κλινικής Ογκολογίας του 2020 (ASCO20).
Μέχρι σήμερα, η συνδυαστική θεραπεία nivolumab και ipilimumab με δύο κύκλους χημειοθεραπείας έχει εγκριθεί σε εννέα χώρες, συμπεριλαμβανομένων των ΗΠΑ, για την πρώτης γραμμής θεραπεία ασθενών με μεταστατικό μη μικροκυτταρικό καρκίνο του πνεύμονα. Η έγκριση από την Ευρωπαϊκή Επιτροπή θα σηματοδοτούσε την τρίτη ένδειξη για συνδυασμούς που βασίζονται στη συνδυαστική θεραπεία nivolumab με ipilimumab στην Ευρωπαϊκή Ένωση, μετά τις προηγούμενες εγκρίσεις για το μεταστατικό μελάνωμα και το προχωρημένο νεφροκυτταρικό καρκίνωμα.
Η Bristol Myers Squibb εκφράζει τις ευχαριστίες της στους ασθενείς και τους ερευνητές που συμμετείχαν στην κλινική μελέτη CheckMate -9LA.