Η οστεοαρθρίτιδα (ΟΑ) είναι μία χρόνια εκφύλιση και καταστροφή του αρθρικού χόνδρου πού προκαλεί βλάβη των αρθρώσεων και των οστών. Προσβάλλει κυρίως τις γυναίκες ηλικίας μεγαλύτερης των 65 ετών. Κύρια κλινική εκδήλωση της νόσου είναι ο πόνος της προσβεβλημένης άρθρωσης, η δυσκαμψία και η μειωμένη λειτουργικότητά της. Στην ανασκόπηση αυτή θα αναφερθούμε στα νεότερα θεραπευτικά δεδομένα για την αντιμετώπιση της νόσου. Η θεραπεία της ΟΑ είναι μακροχρόνια, επίμονη και αρκετά δύσκολη. Κύριος στόχος της θεραπείας είναι η μείωση των συμπτωμάτων, η βελτίωση της λειτουργικότητας της άρθρωσης και της ποιότητας της ζωής των ασθενών και ακόμη η επιβράδυνση των καταστροφικών βλαβών.
Από το Αμερικανικό Κολέγιο Ρευματολογίας (ACR) καθώς και από την επιτροπή της Ευρωπαϊκής Ένωσης κατά του Ρευματισμού (EULAR) εδόθησαν συστάσεις για την αντιμετώπιση της ΟΑ. Σύμφωνα με τις συστάσεις των επιτροπών αυτών, η θεραπευτική προσέγγιση της νόσου χωρίζεται σε τρία μέρη:
1) μη θεραπευτική αντιμετώπιση που περιλαμβάνει κυρίως πρόγραμμα εκπαίδευσης άσκησης και φυσικοθεραπείας,
2) θεραπεία με φάρμακα και
3) χειρουργική αντιμετώπιση που συνίσταται σε αρθροσκοπική αφαίρεση των συντριμμάτων του χόνδρου, οστεοτομία, και ολική αρθροπλαστική. Η θεραπεία με φάρμακα περιλαμβάνει τη χορήγηση απλών αναλγητικών από το στόμα όπως η ακεταμινοφένη, τα αντιφλεγμονώδη μη στεροειδή φάρμακα (ΑΜΣΦ), που είναι τα πλέον χρησιμοποιούμενα φάρμακα στη θεραπεία της ΟΑ, καθώς και τα νεώτερα ΑΜΣΦ που αναστέλλουν το ένζυμο κυκλοοξυγενάση . Τα τελευταία έχουν λιγότερες παρενέργειες από το γαστρεντερικό, και καλή αποτελεσματικότητα. Τέτοια φάρμακα είναι η ροφεκοξίμπη και η σελεκοξίμπη. Από τα νεώτερα φάρμακα, η από του στόματος χορήγηση της διασερεΐνης, της θειικής χονδροϊτίνης και η ενδοαρθρική χορήγηση του υαλουρονικού φαίνεται ότι έχουν θετική επίδραση στον πόνο και βελτιώνουν την κινητικότητα της άρθρωσης. Όμως το φάρμακο που βελτιώνει τον πόνο, επιδρά θετικά στην κινητικότητα της άρθρωσης αλλά επηρεάζει και τις ακτινολογικές αλλοιώσεις της νόσου, είναι η θειική γλυκοζαμίνη και γι’ αυτό μπορεί να θεωρηθεί φάρμακο τροποποιητικό της νόσου.
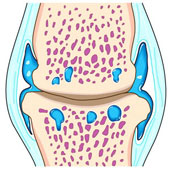
Η οστεοαρθρίτιδα (ΟΑ) είναι μια προοδευτική εκφύλιση του αρθρικού χόνδρου που οδηγεί στην καταστροφή της άρθρωσης και των οστών. Χαρακτηρίζεται από πόνο της προσβεβλημένης άρθρωσης, δυσκαμψία και ελάττωση της κινητικότητας της. Είναι ένα παγκόσμιο πρόβλημα που προσβάλλει 50% των ατόμων ηλικίας >65 ετών και περισσότερο τις γυναίκες. Είναι η πιο συχνή νόσος του μυοσκελετικού συστήματος και αν λάβει κανείς σαν κριτήριο τις ακτινολογικές βλάβες των αρθρώσεων, τότε φαίνεται ότι περισσότερο από 75% των ατόμων μεγαλύτερα των 70 ετών έχουν ακτινογραφικές αλλοιώσεις ΟΑ.
Η ΟΑ προσβάλλει τις αρθρώσεις των χεριών (εγγύς φαλαγγικές, άπω φαλαγγικές) καθώς και την καρπομετακάρπια άρθρωση του αντίχειρα. Άλλες αρθρώσεις που προσβάλλονται πολύ συχνά είναι οι αρθρώσεις της αυχενικής μοίρας της σπονδυλικής στήλης, της οσφυϊκής μοίρας, τα ισχία, τα γόνατα και οι πρώτες μεταταρσοφαλαγγικές αρθρώσεις των ποδιών.
Υπάρχουν αρκετοί παράγοντες που προδιαθέτουν στην ανάπτυξη της ΟΑ, όπως γενετική προδιάθεση των ατόμων (μεταλλάξεις του γονιδίου του κολλαγόνου τύπου ΙΙ), τραύματα, φλεγμονώδης διεργασία της άρθρωσης, βαριά άσκηση, παχυσαρκία, βιοχημικές και μεταβολικές διαταραχές. Η νόσος αρχίζει με προοδευτική εκφύλιση και καταστροφή του αρθρικού χόνδρου, ακολούθως προσβάλλεται το υποκείμενο οστούν, οι παρακείμενοι ιστοί και ο αρθρικός υμένας. Με την καταστροφή του αρθρικού χόνδρου το υποκείμενο οστούν υφίσταται μεγαλύτερη πίεση και αρχίζει σκλήρυνση και σχηματισμός κύστεων. Στη συνέχεια αρχίζει η παραγωγή νέου οστού από τις παρυφές του αρθρικού χόνδρου με αποτέλεσμα το σχηματισμό οστεοφύτων.
Η θεραπεία της ΟΑ είναι δύσκολη, μακροχρόνια και επίμονη. Για να κατανοήσουμε την θεραπευτική παρέμβαση συνοπτικά θα αναφερθούμε στους παθοφυσιολογικούς μηχανισμούς που οδηγούν στην καταστροφή του αρθρικού χόνδρου.
Παθοφυσιολογία οστεοαρθρίτιδας
Ο αρθρικός χόνδρος αποτελείται από τα χονδροκύτταρα και από τη μεσοκυττάρια ουσία (matrix). Τα χονδροκύτταρα είναι πολύ ενεργά κύτταρα, έχουν σχήμα ελικοειδές ή σφαιροειδές, παράγουν και εκκρίνουν την μεσοκυττάρια ουσία στην οποία είναι εμβαπτισμένα. Έχουν υποδοχείς για πολλές κυτταροκίνες όπως ιντερλευκίνη 1 (IL-1), παράγοντα νέκρωσης των όγκων (TNFα), ιντερλευκίνη 4 (IL-4), ιντερλευκίνη 10 (IL-10) και για αυξητικούς παράγοντες όπως ο αυξητικός παράγων της ινσουλίνης (IGF). Η ενεργοποίηση των χονδροκυττάρων, προκαλεί την παραγωγή της μεσοκυττάριας ουσίας και πολλών ενζύμων, τις μεταλλοπρωτεάσες (MMP) και τις σερινοπρωτεάσες (PA) που την αποδομούν. Επιπρόσθετα, από τα ίδια κύτταρα παράγονται ο ιστικός αναστολέας των MMP (TIMP) και ο αναστολέας των σερινοπρωτεασών (PAI) που ελέγχουν τη δράση των ενζύμων αυτών. Έτσι θα πρέπει να υπάρχει μια ισορροπία μεταξύ σύνθεσης και αποδόμησης των διεργασιών αυτών για την καλή ομοιοστασία του αρθρικού χόνδρου.
Η μεσοκυττάριος ουσία αποτελείται:
α) από τις γλυκοσαμινογλυκάνες,
β) από ίνες κολλαγόνου και
γ) από μη κολλαγονικές πρωτεΐνες. Κάθε μόριο γλυκοσαμινογλυκάνης αποτελείται από μια κεντρική πρωτεΐνη που λέγεται protein core filament, στο τέλος αυτής υπάρχει μια άλλη πρωτεΐνη που λέγεται συνδετική πρωτεΐνη (link protein), που συνδέει την κεντρική πρωτεΐνη με την υαλουρονάνη (ΥΑ) ή υαλουρανικό οξύ. Στο πλάγιο της κεντρικής πρωτεΐνης συνδέονται άλλες αμινογλυκάνες, όπως η θειική χονδροϊτίνη, η θειική γλυκοζαμίνη και άλλες που είναι αρνητικά φορτισμένες και κρατούν μεγάλες ποσότητες νερού. Η μεγάλη ποσότητα του νερού που κατακρατείται από τα μόρια των αμινογλυκανών, έχει σαν αποτέλεσμα ο χόνδρος να ανθίσταται και να μην καταστρέφεται στις διάφορες πιέσεις που δέχεται. Έτσι σε μεγάλη πίεση του αρθρικού χόνδρου τα μόρια του νερού απελευθερώνονται και επανέρχονται όταν ελαττωθεί ή φύγει η πίεση που ασκείται.
Η μεσοκυττάριος ουσία δηλαδή, λειτουργεί σαν «σφουγγάρι» ή σαν «αμορτισέρ» αυτοκινήτου ελαττώνοντας τους «κραδασμούς» που ασκούνται στον χόνδρο.
Το κολλαγόνο της μεσοκυττάριας ουσίας είναι τύπου ΙΙ σε ποσοστό 97%, ενώ κολλαγόνο τύπου ΙΧ και ΧΙ ανευρίσκεται σε ποσοστό 2-3%.
Όπως αναφέρθηκε προηγουμένως, υπάρχουν πολλοί παράγοντες που επηρεάζουν και αλλάζουν την ομοιοστασία και τη λειτουργία του αρθρικού χόνδρου. Οι παράγοντες αυτοί διεγείρουν και ενεργοποιούν τα χονδροκύτταρα, με αποτέλεσμα παραγωγή προφλεγμονωδών κυτταροκινών (IL-1 και TNFα) που προάγουν την παραγωγή των MMP και PA με αποτέλεσμα αυξημένη καταβολική ιδιότητα. Φυσιολογικά η μεγάλη δραστηριότητα των MMP και PA αναστέλλεται από τους αναστολείς τους. Όμως, μελέτες έχουν δείξει ότι οι αναστολείς αυτοί (TIMP, ΡΑ) δεν λειτουργούν φυσιολογικά στην ΟΑ και υπερτερούν οι καταβολικές διεργασίες.
Επίσης η δραστηριότητα των αντιφλεγμονωδών κυτταροκινών (IL-4, IL-10) είναι μειωμένη. Αυτό έχει σαν αποτέλεσμα αυξημένη αποδόμηση και καταστροφή των γλυκοσαμινογλυκανών και των μορίων του κολλαγόνου. Έτσι, τα μόρια των γλυκοσαμινογλυκανών και του κολλαγόνου που παραμένουν ή που αναδομούνται δεν είναι το ίδιο ανθεκτικά, συγκρατούν μεγάλες ποσότητες νερού και αρχίζει η καταστροφή του χόνδρου (Εικόνα 2). Θραύσματα χόνδρου πέφτουν στο αρθρικό υγρό (AY), με αποτέλεσμα ενεργοποίηση των πολυμορφοπύρηνων κυττάρων και φαγοκυττάρωση. Επέρχεται δευτεροπαθής φλεγμονώδης αντίδραση του αρθρικού υμένα και συνεχής παραγωγή προφλεγμονωδών κυτταροκινών. Ακολουθεί ενεργοποίηση του συστήματος της βραδυκινίνης, η ενεργοποίηση της φωσφολιπάσης Α2 της κυτταρικής μεμβράνης των χονδροκυττάρων και υμενοκυττάρων και συνεχίζει ο καταρράκτης ενεργοποίησης του αραχιδονικού οξέος με την ενεργοποίηση της κυκλοοξυγενάσης 1 (COX-1) και κυκλοοξυγενάσης 2 (COX-2) με αποτέλεσμα παραγωγή προσταγλανδινών και άλλων μεσολαβητών της φλεγμονής. Αυτό έχει σαν αποτέλεσμα συνεχή αποδόμηση της μεσοκυττάριας ουσίας και έτσι επέρχεται περαιτέρω καταστροφή του αρθρικού χόνδρου και του υποκείμενου οστού.5,6
Ο κύριος στόχος της θεραπευτικής παρέμβασης της ΟΑ είναι: α) Η μείωση των συμπτωμάτων, β) βελτίωση της λειτουργικότητας της άρθρωσης και της ποιότητας ζωής των ασθενών και γ) αναχαίτιση ή επιβράδυνση των καταστροφικών διεργασιών. Πρόσφατα από το Αμερικανικό Κολέγιο Ρευματολογίας (ACR)8 και από την Επιτροπή της Ευρωπαϊκής Ένωσης κατά του Ρευματισμού (EULAR)9 εδόθησαν συστάσεις για την αντιμετώπιση της ΟΑ, με ορισμένες διαφορές μεταξύ των δύο επιτροπών. Για παράδειγμα, από το ACR δεν συνιστώνται στη θεραπεία της ΟΑ τα νέα τροποποιητικά φάρμακα που πιθανόν αναχαιτίζουν τη νόσο όπως η διασερεΐνη και η θειική γλυκοζαμίνη. Αντίθετα, τα φάρμακα αυτά συνιστώνται από την επιτροπή της EULAR.
Σύμφωνα με τις συστάσεις η θεραπευτική προσέγγιση της ΟΑ μπορεί να χωριστεί σε τρία μέρη:
1) μη θεραπευτική αντιμετώπιση η οποία περιλαμβάνει κυρίως την εκπαίδευση του ασθενή, προγράμματα άσκησης, απώλεια βάρους, φυσικοθεραπεία, κλπ,
2) θεραπεία με φάρμακα που χορηγούνται από το στόμα, ενδοαρθρικά ή τοπικά και τέλος
3) χειρουργική αντιμετώπιση.
Η μη θεραπευτική αντιμετώπιση αποτελεί τον ακρογωνιαίο λίθο στην αντιμετώπιση της ΟΑ και πρέπει να εφαρμόζεται πάντα. Μπορεί να μειώσει τον πόνο, να βελτιώσει την κινητικότητα και να μειώσει την χρήση των αναλγητικών και των άλλων φαρμάκων. Περιλαμβάνει την εκπαίδευση του ασθενούς, πρόγραμμα κοινωνικής υποστήριξης, μείωση του σωματικού βάρους εφ’ όσον χρειάζεται, ασκήσεις αεροβικής γυμναστικής, προγράμματα φυσικοθεραπείας, εργοθεραπείας κλπ .
Η θεραπευτική αντιμετώπιση, σύμφωνα με το ACR, περιλαμβάνει φάρμακα και άλλες παρεμβάσεις που φαίνονται στον πίνακα 2. Από τα πιο απλά φάρμακα το περισσότερο χρησιμοποιούμενο είναι η ακεταμινοφένη, η οποία χορηγείται από το στόμα σε δόση μέχρι 4 gr/ημέρα. Οι αρχικές μελέτες έδειξαν ότι δεν υπήρχε διαφορά μεταξύ ακεταμινοφένης και αντιφλεγμονωδών μη στεροειδών φαρμάκων (ΑΜΣΦ). Όμως, νεότερες μελέτες έδειξαν ότι τα ΑΜΣΦ έχουν καλύτερη αποτελεσματικότητα από την ακετομινοφένη. Όταν οι ασθενείς δεν ανταποκρίνονται σε απλά αναλγητικά τότε χορηγούνται ΑΜΣΦ. Τα ΑΜΣΦ είναι τα φάρμακα που χρησιμοποιούνται περισσότερο στη θεραπεία της ΟΑ, τόσο στην κλινική πράξη καθώς και σε κλινικές μελέτες. Όπως είναι γνωστό, τα κλασικά ΑΜΣΦ αναστέλλουν κυρίως την COX-1 και λιγότερο την COX-2.
Επειδή η COX-1 είναι δομικό ένζυμο χρήσιμο για την παραγωγή προσταγλανδινών που είναι ωφέλιμες για τη λειτουργία πολλών οργάνων (στομάχου, νεφρών, αιμοπεταλίων), η αναστολή της έχει πολλές επιπτώσεις στα παραπάνω όργανα. Σε ηλικιωμένους ασθενείς, οι παρενέργειες αυτές αυξάνονται, γι’ αυτό τα κλασικά ΑΜΣΦ θα πρέπει να χορηγούνται με προσοχή στα άτομα αυτά.
Έτσι, η χορήγηση ΑΜΣΦ αντενδείκνυται σε άτομα με ιστορικό υπέρτασης, έκπτωσης νεφρικής λειτουργίας, συμφορητικής καρδιακής ανεπάρκειας, σύγχρονης θεραπείας με διουρητικά ή αναστολείς του μετατρεπτικού ενζύμου της αγγειοτενσίνης. Σε άτομα με αυξημένο κίνδυνο παρενεργειών από το γαστρεντερικό θα πρέπει να χορηγούνται και γαστροπροστατευτικά φάρμακα που είναι η μισοπροστόλη ή οι αναστολείς της αντλίας πρωτονίων.
Σήμερα για να αποφύγουμε τις παραπάνω παρενέργειες χρησιμοποιούνται ΑΜΣΦ με μεγαλύτερη εκλεκτικότητα αναστολής της COX-2, η οποία είναι μια επαγόμενη πρωτεΐνη που παράγεται μετά από φλεγμονώδη ερεθίσματα και είναι η κύρια πρωτεΐνη παραγωγής προσταγλανδινών που επάγουν την φλεγμονή. Η χρησιμοποίηση ΑΜΣΦ που αναστέλλουν κυρίως την COX-2, και λιγότερο την COX-1, έχει σαν αποτέλεσμα ελάττωση της φλεγμονώδους διεργασίας και λιγότερο επηρεασμό των προσταγλανδικών που προέρχονται από την COX-1. Σαν συνέπεια παρατηρούνται λιγότερες παρενέργειες από το γαστρεντερικό και τα νεφρά. Τέτοια φάρμακα είναι η νιμεσουλίδη, η μελοξικάμη, η ναμπουμετόνη και άλλα. Επίσης, χρησιμοποιούνται και ΑΜΣΦ που εκλεκτικά αναστέλλουν την COX-2 με αποτέλεσμα λιγότερες παρενέργειες από το γαστρεντερικό. Τα φάρμακα αυτά λέγονται κοξίμπες και είναι η ροφεκοξίμπη και η σελεκοξίμπη.
Επίσης, μελέτες έδειξαν ότι τα νέα ΑΜΣΦ με εκλεκτική δράση στην COX-2 δεν έχουν και μεγαλύτερη αποτελεσματικότητα, όσον αφορά τη φλεγμονώδη διεργασία και ορισμένοι υποστηρίζουν ότι η αποτελεσματικότητά τους είναι μικρότερη.
Μολονότι οι εκλεκτικοί αναστολείς της COX-2 είναι πιο ασφαλή φάρμακα για το γαστρεντερικό συγκριτικά με τα κλασικά ΑΜΣΦ, εν τούτοις δεν προστατεύουν από τα καρδιακά συμβάματα και μπορεί να επιδεινώσουν τη νεφρική λειτουργία. Έτσι, στη μελέτη VIGOR βρέθηκε ότι η συχνότητα εμφάνισης εμφράγματος του μυοκαρδίου ήταν μεγαλύτερη στην ομάδα της ροφεκοξίμπης συγκριτικά με εκείνη της ναπροξένης.
Αυτό συμβαίνει γιατί οι εκλεκτικοί αναστολείς της COX-2 ελαττώνουν την παραγωγή της προστακυκλίνης η οποία ως γνωστό παρεμβαίνει αναστέλλοντας τη συγκόλληση των αιμοπεταλίων. Από την άλλη μεριά η COX-2 εκφράζεται φυσιολογικά στα αγγεία των νεφρών καθώς και στα κύτταρα του φλοιού και μυελού του νεφρικού παρεγχύματος. Η έκφραση δε αυτή της COX-2 στο νεφρό αυξάνεται με την ηλικία, γι’ αυτό η αναστολή της COX-2 μπορεί να προκαλέσει κατακράτηση υγρών, οιδήματα, υπέρταση και έκπτωση της νεφρικής λειτουργίας.
Συνεπώς και οι εκλεκτικοί αναστολείς της COX-2 θα πρέπει να χορηγούνται με μεγάλη προσοχή σε ηλικιωμένα άτομα, σε ασθενείς με καρδιοαγγειακά συμβάματα, υπέρταση και έκπτωση της νεφρικής λειτουργίας.
Σήμερα υπάρχουν πολλές ενδείξεις ότι ορισμένα φάρμακα που λέγονται τροποποιητικά της νόσου, μπορεί να επιβραδύνουν ή/και να αναχαιτίσουν την εξέλιξη της ΟΑ. Τα φάρμακα αυτά είναι η διασερεΐνη, η θειική γλυκοζαμίνη και η θειική χονδροϊτίνη, το υαλουρονικό οξύ και άλλα.10
Η διασερεΐνη είναι ένα φάρμακο που αναστέλλει τη δράση της IL-1 και των MMPs in vitro. Στα πειραματόζωα μετά από ένεση καραγενάσης και την ανάπτυξη οιδήματος πέλματος, η χορήγηση διασερεΐνης ελάττωσε σημαντικά τη φλεγμονώδη αντίδραση.
Σε μια πρόσφατη διπλή-τυφλή, τυχαιοποιημένη με εικονικό φάρμακο μελέτη έλαβαν μέρος 484 ασθενείς με ΟΑ γόνατος. Οι ασθενείς ελάμβαναν σε παράλληλη χορήγηση τρεις διαφορετικές δόσεις διασερεΐνης (50, 100, 150 mg/ημέρα, χορηγούμενη δύο φορές την ημέρα) για διάστημα 16 εβδομάδων. Χρησιμοποιώντας σαν πρωταρχικό κριτήριο την εκτίμηση του πόνου, σύμφωνα με το κριτήριο της οπτικής αναλογικής κλίμακας, βρέθηκε ότι η διασερεΐνη στη δόση των 100 mg/ημέρα (50 mg x 2) βελτίωσε τα συμπτώματα του πόνου στους ασθενείς αυτούς.
Η γλυκοζαμίνη, όπως αναφέρθηκε προηγουμένως, είναι ένα φυσικό συστατικό των γλυκοζαμινογλυκανών του αρθρικού χόνδρου. Η θειική γλυκοζαμίνη είναι ένα θειικό παράγωγο της γλυκοζαμίνης και η οποία χορηγούμενη από το στόμα βρέθηκε ότι έχει ευεργετικά αποτελέσματα στον πόνο στους ασθενείς με ΟΑ.18 Σε μία πρόσφατη μακροχρόνια μελέτη διάρκειας 3 ετών συγκρίθηκε η αποτελεσματικότητα και η ασφάλεια της θειικής γλυκοζαμίνης με εικονικό φάρμακο σε ασθενείς με ΟΑ του γόνατος. Μελετήθηκαν 212 ασθενείς. Από αυτούς 106 τυχαιοποιήθηκαν να παίρνουν θειική γλυκοζαμίνη 1500 mg μια φορά την ημέρα από το στόμα και 106 έπαιρναν εικονικό φάρμακο.
Έγιναν ακτινογραφίες γονάτων σε όρθια θέση κατά την έναρξη της μελέτης, μετά από ένα και 3 χρόνια. Υπολογίστηκε με απεικονιστική ψηφιακή ανάλυση το μέσο εύρος του μέσου διαμερίσματος του μεσάρθριου διαστήματος, ενώ το ελάχιστο εύρος της άρθρωσης, στο πιο στενό σημείο, μετρήθηκε ξεχωριστά με μεγεθυντικό φακό. Τα κλινικά συμπτώματα εκτιμήθηκαν σύμφωνα με το δείκτη κατά WOMAC. Μετά την πάροδο των 3 ετών, στην ομάδα με το εικονικό φάρμακο υπήρχε μια προοδευτική ελάττωση του μεσάρθριου διαστήματος της τάξεως του
-0,31 mm, ενώ δεν υπήρχε ελάττωση του μεσάρθριου διαστήματος στους ασθενείς της θειικής γλυκοζαμίνης (-0,06 mm). Τα κλινικά συμπτώματα (πόνος, κινητικότητα) χειροτέρευσαν στην ομάδα με το εικονικό φάρμακο συγκριτικά με την ομάδα της θειικής γλυκοζαμίνης. Δεν υπήρχε διαφορά μεταξύ των δύο ομάδων όσον αφορά την ανεκτικότητα και την ασφάλεια του φαρμάκου. Συμπεραίνεται ότι η θειική γλυκοζαμίνη μπορεί να επηρεάσει την εξέλιξη της νόσου.
Ένα άλλο συστατικό των γλυκοζαμινογλυκανών του αρθρικού χόνδρου είναι και η θειική χονδροϊτίνη. Η χορήγηση της θειικής χονδροϊτίνης από το στόμα φαίνεται ότι έχει ευεργετικά αποτελέσματα όσον αφορά τον πόνο και την κινητικότητα σε ασθενείς με ΟΑ γόνατος. Όμως δεν υπάρχουν μακροχρόνιες μελέτες που να επιβεβαιώνουν ότι η θειική χονδροϊτίνη μπορεί να επιβραδύνει την εξέλιξη της ΟΑ.21
Η υαλουρονάνη είναι μια μεγάλου μοριακού βάρους γλυκοζαμινογλυκάνη που αποτελείται από επαναλαμβανόμενους δισακχαρίτες του γλυκουρονικού οξέος και Ν-ακετυλογλυκοζαμίνης. Παράγεται από τα υμενοκύτταρα και τα χονδροκύτταρα και προσδίδει στο ΑΥ υψηλή γλοιότητα. Επιδρά στην ροή του ΑΥ αυξάνοντας τις ιξοδοελαστικές ιδιότητές του, ενώ έχει την ικανότητα να δρα σαν «χημικό σφουγγάρι» που καθαρίζει μακρομοριακά τεμάχια κι άλλα «απόβλητα» της παθολογικής άρθρωσης. Εξαιτίας των ιδιοτήτων αυτών θεωρήθηκε ότι η ΥΑ χορηγούμενη ενδοαρθρικά θα μπορούσε να βελτιώσει την ιξοδοελαστικότητα της παθολογικής άρθρωσης, να βελτιώσει τη ροή του ΑΥ, να ομαλοποιήσει την παραγωγή της ενδογενούς ΥΑ και να ελαττώσει τον πόνο.
Σε μία πρόσφατη ανασκόπηση και μετά-ανάλυση των εργασιών σχετικά με την ενδοαρθρική χορήγηση ΥΑ συμπεραίνεται ότι η ΥΑ επιδρά θετικά στη ελάττωση του πόνου, η δράση της μπορεί να διαρκέσει αρκετούς μήνες, όμως δεν φαίνεται να τροποποιεί την εξέλιξη της νόσου.
Η χειρουργική αντιμετώπιση συνιστάται σε βαριά ΟΑ, χωρίς υποχώρηση του πόνου με τη θεραπεία και περιορισμό της κινητικότητας της άρθρωσης, συνίσταται σε:
1) αρθροσκοπική αφαίρεση των συντριμμάτων του χόνδρου,
2) οστεοτομία και
3) ολική αρθροπλαστική. Η έκβαση της χειρουργικής αντιμετώπισης εξαρτάται από το χρόνο διενέργειας της επέμβασης, την εμπειρία του ορθοπεδικού, το νοσοκομείο, την προεγχειρητική κατάσταση του ασθενούς, τη μετεγχειρητική αντιμετώπιση και τη φυσικοθεραπεία.
Τέλος, οι υπάρχουσες μελέτες σχετικά με τη χρήση του βελονισμού στη θεραπεία της ΟΑ δείχνουν ότι η βελονοθεραπεία έχει κάποια ευεργετική επίδραση στον πόνο, όμως δεν έχει καμιά επίδραση στην κινητικότητα και την ποιότητα ζωής των ασθενών αυτών.
Συμπερασματικά φαίνεται ότι όλα τα φάρμακα τα οποία προτείνονται από το ACR και από την EULAR, για τη θεραπεία της ΟΑ έχουν ευεργετική δράση κυρίως στον πόνο και λιγότερο στην κινητικότητα της άρθρωσης και καθόλου στην εξέλιξη της νόσου. Η θειική γλυκοζαμίνη όμως είναι το μόνο φάρμακο που μπορεί να βελτιώσει τα συμπτώματα, την κινητικότητα της άρθρωσης άλλα και να επιβραδύνει την εξέλιξη της νόσου για αυτό μπορεί να θεωρηθεί σαν ένα φάρμακο τροποποιητικό της ΟΑ.
Αλέξανδρος Α. Δρόσος, Καθηγητής Παθολογίας/Ρευματολογίας
Ιατρική Σχολή Πανεπιστημίου Ιωαννίνων
Ο κ. Αλέξανδρος Α. Δρόσος είναι Καθηγητής Παθολογίας/Ρευματολογίας και Δ/ντής της Ρευματολογικής Κλινικής του Πανεπιστημιακού Νοσοκομείου Ιωαννίνων. Έλαβε το πτυχίο της Ιατρικής από την Ιατρική Σχολή του Πανεπιστημίου του Μπάρι στην Ιταλία. Το 1983 ολοκλήρωσε την ειδίκευσή του στην Εσωτερική Παθολογία και το 1984 ορκίστηκε Διδάκτωρ της Ιατρικής Σχολής του Πανεπιστημίου Ιωαννίνων. Το 1986 έλαβε την ειδικότητα της ρευματολογίας. Μετεκπαιδεύτηκε στο Guy’s Hospital του Λονδίνου και στο National Institutes for Health, National Institute of Neurological Disorders and Stroke στην Bethesda των Ηνωμένων Πολιτειών. Ο Καθηγητής κ. Δρόσος έχει δημοσιεύσει περισσότερα από 210 άρθρα σε διεθνή περιοδικά. Τα τελευταία χρόνια το ερευνητικό του ενδιαφέρον επικεντρώνεται στην επιδημιολογία των αυτοάνοσων ρευματικών νοσημάτων και στους προγνωστικούς παράγοντες της ρευματοειδούς αρθρίτιδας και των σπονδυλοαρθροπαθειών καθώς και την απόκρισή τους στη θεραπεία.
Θα ήθελα να ευχαριστήσω την κα. Ελένη Χόρτη και τον κ. Σπύρο Βούλγαρη για τη γραμματειακή υποστήριξη.
Βιβλιογραφία
1. Peyron SG. Epidemiologic and etiologic approach to osteoarthritis. Sem Arthritis Rheum 1979, 8:286–306
2. Felson DT and Zhang Y. An update on the epidemiology of knee and hip osteoarthritis with a view to prevention. Arthritis Rheum 1998, 41:1343–1359
3. Felson DT, Naimark A, Anderson J et al. The prevalence of knee osteoarthritis in the elderly. The Framingham osteoarthritis study. Arthritis Rheum 1987, 30:914–918
4. Felson DT. NIH Conference: Osteoarthritis: new insights Part 1: The disease and its risk factors. Ann Intern Med 2000, 133:635–646
5. Goldring MB. The role of chondrocyte in osteoarthritis. Arthritis Rheum 2000, 43:1916–1926
6. Pelletier JP, Martel-Pelletier, Abramsοn SB. Osteoarthritis, an inflammatory disease. Arthritis Rheum 2001, 44:1237–1247
7. Dean DD, Martel-Pelletier J, Pelletier JP et al. Evidence for metalloproteinase and metalloproteinase inhibitor imbalance in human osteoarthritis cartilage. J Clin Invest 1989, 84:678–685
8. American college of Rheumatology subcommittee on osteoarthritis guidelines. Recommendations for the medical management of osteoarthritis of the hip and knee 2000 update. Arthritis Rheum 2000, 43:1905–1915
9. Pendleton A, Arden N, Dougados M et al. EULAR recommendations for the management of knee osteoarthritis: report of task force of the standing committee for international clinical studies including therapeutic trials (ESCISIT). Ann Rheum Dis 2000, 43:936–944
10. Felson DT. NIH Conference: Osteoarthritis: new insights Part 2: Treatment approaches. Ann Intern Med 2000, 133:726–737
11. Wolfe MM, Lichtenstein DR, Singh G. Gastrointestinal toxicity of nonsteroidal antiinflammatory drugs. N Engl J Med 1999, 340:1888–1899
12. Silverstein FE, Faich G, Goldstein JL et al. Gastrointestinal toxicity with celecoxib vs non steroidal anti-inflammatory drugs for osteoarthritis and rheumatoid arthritis: the CLASS study: a randomized controlled trial. Celecoxib long-term arthritis safety study. JAMA 2000, 284: 1247–1255
13. Bombardier C, Laine L, Reicin Α et al. Comparison of upper gastrointestinal toxicity of refecoxib and naproxen in patients with rheumatoid arthritis. N Engl J Med 2000, 343:1520–1528
14. Swan SK, Rudy DW, Lassester K et al. Effect of cycloxygenase-2 inhibition on renal function in elderly persons receiving a low-salt diet. Ann Intern Med 2000, 133:1–9
15. FitzGerald GA and Patrono C. The coxibs, selective inhibitors of cyclooxygenase 2. N Engl J Med 2001, 345:433–442
16. Boers M. NSAIDs and selective COX-2 inhibitors: Competition between gastroprotection and cardioprotection. Commentary. Lancet 2001, 357:1222–1223
17. Pelletier JP, Yaron M, Haraoui B et al. Efficacy and safety of diacerein in osteoarthritis of the knee. Arthritis Rheum 2000, 43:2339–2348
18. Deal CL and Moskowitz RW. Nutraceuticals as therapeutic agents in osteoarthritis: the role of glucosamine, chondroitin sulfate, and collagen hydrolysate. Rheum Dis Clin North Am 1999, 25:379–395
19. Reginster Y, Deroisy R, Rovati L et al. Long term effects of glucosamine on osteoarthritis progression: a randomized, placebo-controlled clinical trial. Lancet 2001, 357:251–256
20. McAlindon M. Glucosamine for osteoarthritis: dawn of a new era? Editorial. Lancet 2001, 357:247
21. Leeb BF, Schweitzer H, Montac K et al. A meta-analysis of chondroitin sulfate in the treatment of osteoarthritis. J Rheumatol 2000, 27:205–211
22. Balazs EA and Denlinger JL. Viscosupplementation: a new concept in the treatment of osteoarthritis. J Rheumatol 1993, 20(suppl 39):3–9
23. Brandt KD, Smith GN Jr, Simon LS. Intraarticular injection of hyaluronan as treatment for knee osteoarthritis: what is the evidence? Arthritis Rheum 2000, 43:1192–1203
24. Ezzo J, Hadhazy V, Birch S et al. Acupuncture for osteoarthritis of the knee. Arthritis Rheum 2001, 44:819–825